�߿����W(xu��)��݆��(f��)��(x��)����(y��ng)���ʺͻ��W(xu��)ƽ�⌣�}���Y(ji��)
2019-01-08 16:06:37���þW(w��ng)
�����Ŷ��x���Á��������W(xu��)����(y��ng)�Ŀ�������λ�r�g��(n��i)����(y��ng)�������������|(zh��)������׃��
�����Ʊ�ʾ��������λ�r�g��(n��i)����(y��ng)��ȵĜp�ٻ��������ȵ����Ӂ���ʾ
������Ӌ(j��)�㹫ʽ��v=Δc/Δt(υ��ƽ�����ʣ�Δc�����׃����Δt���r�g)��λ��mol/(L·s)
������Ӱ����أ�
�����ٛQ������(��(n��i)��)������(y��ng)������|(zh��)(�Q������)
�����ڗl������(����)������(y��ng)��̎�ėl��
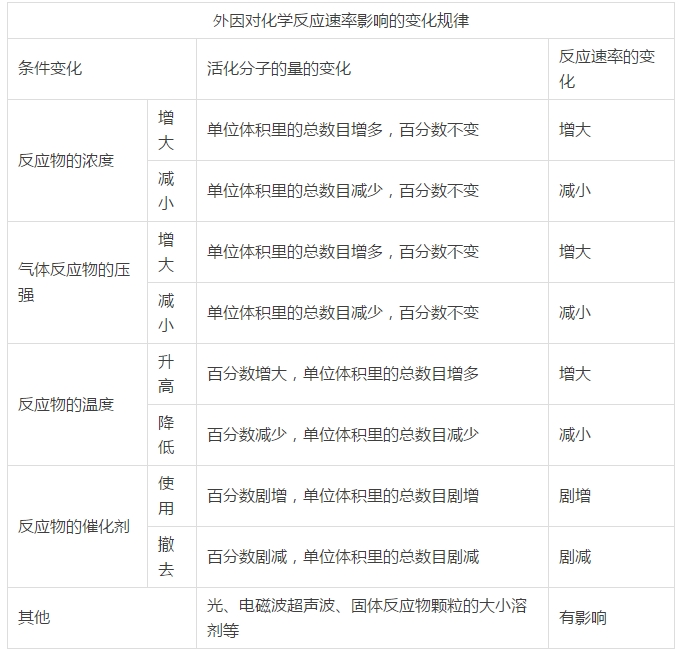
����ע�⣺
����(1)���ӷ���(y��ng)�����|(zh��)����w��Һ�w�����ډ���(qi��ng)��׃������Ȏ��oӰ푣������J(r��n)�鷴��(y��ng)���ʲ�׃��
����(2)���Ԛ��w�������ʵ�Ӱ�
�����ٺ�غ��ݕr��������Ԛ��w→���������Ǹ��։���׃�������|(zh��)��Ȳ�׃→����(y��ng)���ʲ�׃
�����ں�غ��w�r��������Ԛ��w→�w�e����→������(y��ng)���ȜpС→����(y��ng)���ʜp��
�������W(xu��)ƽ��֪�R�c(di��n)���Y(ji��)
����1�����x��
�������W(xu��)ƽ���B(t��i)��һ���l���£���(d��ng)һ�����淴��(y��ng)�M(j��n)�е����淴��(y��ng)������ȕr�����M�ɳɷ֝�Ȳ��ٸ�׃���_(d��)���������oֹ��һ�N“ƽ��”���@�����@������(y��ng)�����_(d��)�����ȼ����W(xu��)ƽ���B(t��i)��
����2�����W(xu��)ƽ�������
������(�о�ǰ���ǿ��淴��(y��ng))
������(ͬһ���|(zh��)�����淴��(y��ng)�������)
������(�ӑB(t��i)ƽ��)
������(�����|(zh��)�ĝ���c�|(zh��)����?j��n)?sh��)�㶨)
����׃(�l����׃��ƽ��l(f��)��׃��)
����3���Д�ƽ�������(j��)
�����Д���淴��(y��ng)�_(d��)��ƽ���B(t��i)�ķ���������(j��)
�����D1-2
����4��Ӱ푻��W(xu��)ƽ���Ƅӵ�����
����(һ)��Ȍ����W(xu��)ƽ���Ƅӵ�Ӱ�
����(1)Ӱ�Ҏ(gu��)�ɣ��������l����׃����r�£�����(y��ng)��ĝ�Ȼ�p��������ĝ�ȣ�������ʹƽ�����������Ƅ�;����������ĝ�Ȼ�pС����(y��ng)��ĝ�ȣ�������ʹƽ�����淽���Ƅ�
����(2)���ӹ��w��Һ�w���������ڝ�Ȳ�׃������ƽ�ⲻ�Ƅ�
����(3)����Һ���M(j��n)�еķ���(y��ng)�����ϡ���Һ������(y��ng)���ȜpС����������Ҳ�pС��V���pС��V��Ҳ�pС�����ǜpС�ij̶Ȳ�ͬ�����ĽY(ji��)���ǻ��W(xu��)ƽ����(y��ng)����ʽ�л��W(xu��)Ӌ(j��)����(sh��)֮�ʹ�ķ����Ƅӡ�
����(��)�ضȌ����W(xu��)ƽ���Ƅӵ�Ӱ�
����Ӱ�Ҏ(gu��)�ɣ��������l����׃����r�£��ض����ߕ�ʹ���W(xu��)ƽ���������ᷴ��(y��ng)�����Ƅӣ��ضȽ��͕�ʹ���W(xu��)ƽ�������şᷴ��(y��ng)�����Ƅӡ�
����(��)����(qi��ng)�����W(xu��)ƽ���Ƅӵ�Ӱ�
����Ӱ�Ҏ(gu��)�ɣ������l����׃�r������(qi��ng)����ʹƽ�������w�e�sС�����Ƅ�;�pС����(qi��ng)����ʹƽ�������w�e�������Ƅӡ�
����ע�⣺
����(1)��׃����(qi��ng)����ʹ�o��B(t��i)���|(zh��)���ڵĻ��W(xu��)ƽ��l(f��)���Ƅ�
����(2)���w�p���������c��Һϡጻ��s�Ļ��W(xu��)ƽ���Ƅ�Ҏ(gu��)������
����(��)���������W(xu��)ƽ���Ӱ푣�
��������ʹ�ô�����������(y��ng)���ʺ��淴��(y��ng)����Ӱ푵ij̶��ǵ�ͬ�ģ�����ƽ�ⲻ�Ƅӡ�����ʹ�ô�������Ӱ푿��淴��(y��ng)�_(d��)��ƽ�������_�r�g_��
����(��)��������ԭ��(ƽ���Ƅ�ԭ��)��
���������׃Ӱ�ƽ��ėl��֮һ(��ضȣ�����(qi��ng)�����)��ƽ�������܉�p���@�N��׃�ķ����Ƅӡ�
����5�����W(xu��)ƽ�ⳣ��(sh��)
����(һ)���x��
������һ���ض��£���(d��ng)һ������(y��ng)�_(d��)�����W(xu��)ƽ��r���������ȃ�֮�e�c����(y��ng)���ȃ�֮�e�ı�ֵ��һ������(sh��)��ֵ����̖��K
����(��)ʹ�û��W(xu��)ƽ�ⳣ��(sh��)K��(y��ng)ע��Ć��}��
����1�����_(d��)ʽ�и����|(zh��)�ĝ����׃���ĝ�ȣ�������ʼ���Ҳ�������|(zh��)������
����2��Kֻ�c�ض�(T)�P(gu��n)���c����(y��ng)���������ĝ�ȟo�P(gu��n)��
����3������(y��ng)������a(ch��n)�����й��w��Һ�w���ڕr�����������ǹ̶���׃�ģ����Կ�����“1”�������빫ʽ��
����4��ϡ��Һ���M(j��n)�еķ���(y��ng)������ˮ���ӣ�ˮ�ĝ�Ȳ��،���ƽ���P(gu��n)ϵʽ�С�
����(��)���W(xu��)ƽ�ⳣ��(sh��)K�đ�(y��ng)��:
����1�����W(xu��)ƽ�ⳣ��(sh��)ֵ�Ĵ�С�ǿ��淴��(y��ng)�M(j��n)�г̶ȵĘ�(bi��o)־��KֵԽ���f��ƽ��r������ĝ��Խ����������(y��ng)�M(j��n)�еij̶�Խ��ԓ����(y��ng)�M(j��n)�е�Խ��ȫ������(y��ng)���D(zhu��n)����Խ�ߡ���֮���t�෴��
����2����������Kֵ����(bi��o)��(zh��n)���Д������M(j��n)�еĿ��淴��(y��ng)�Ƿ�ƽ�⼰��ƽ��r��η��M(j��n)�н���ƽ�⡣(Q����ȷe)Q��K������(y��ng)��������(y��ng)�����M(j��n)��;Q=K������(y��ng)̎��ƽ���B(t��i);Q��K������(y��ng)���淴��(y��ng)�����M(j��n)�С�
����3������Kֵ���Д෴��(y��ng)�ğ�Ч��(y��ng)
�������ض����ߣ�Kֵ���t������(y��ng)�����ᷴ��(y��ng)���ض����ߣ�Kֵ�pС���t������(y��ng)��şᷴ��(y��ng)��














