�߿����W(xu��)�_�̣����W(xu��)����(y��ng)����֪�R���Y(ji��)
2018-12-28 21:31:34���þW(w��ng)
����һ�����W(xu��)����(y��ng)����
����1����ʾ����
����ͨ���Æ�λ�r�g��(n��i)����(y��ng)���ȵĜp�ٻ��������ȵ����Ӂ���ʾ��
����2����(sh��)�W(xu��)���_ʽ����λ

����3��Ҏ(gu��)��
����ͬһ����(y��ng)��ͬһ�r�g��(n��i)���ò�ͬ���|(zh��)����ʾ�ķ���(y��ng)���ʿ��ܲ�ͬ��������(y��ng)���ʵĔ�(sh��)ֵ֮�ȵ����@Щ���|(zh��)�ڻ��W(xu��)����ʽ�еĻ��W(xu��)Ӌ����(sh��)֮�ȡ�
����4��ע�����
����(1)��������(y��ng)���ʕr��(y��ng)ָ�����w���|(zh��)��
����(2)һ����f�����W(xu��)����(y��ng)�����S����(y��ng)���M�ж���u�p����ijһ�Εr�g��(n��i)�ķ���(y��ng)���ʣ����H����һ�Εr�g��(n��i)��ƽ�����ʣ�������ָ˲�r���ʡ�
����(3)�oՓ�Ƿ���(y��ng)��߀��������仯�W(xu��)����(y��ng)����ֵ��ȡ��ֵ��
����(4)����һ�����W(xu��)����(y��ng)������|(zh��)֮�g���W(xu��)Ӌ����(sh��)��һ����ͬ�����ԣ���ͬһ�����W(xu��)����(y��ng)��ò�ͬ���|(zh��)��ʾ�Ļ��W(xu��)����(y��ng)���ʲ�һ����ͬ�����ǣ������|(zh��)�Ļ��W(xu��)����(y��ng)����֮�ȵ��������Ļ��W(xu��)Ӌ����(sh��)֮�ȡ�
����(5)���w��Һ�w(ע�⣺������Һ)�����|(zh��)������ȿ�ҕ�鲻׃�ij���(sh��)��һ�㲻���ڱ�ʾ���W(xu��)����(y��ng)���ʡ�
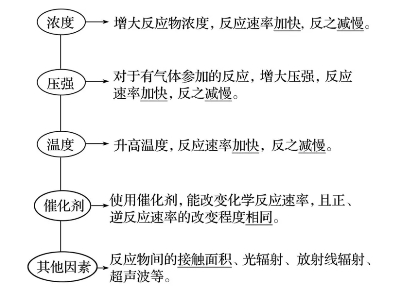
��������Ӱ푻��W(xu��)����(y��ng)���ʵ�����
����1����(n��i)��(��Ҫ����)
��������(y��ng)�ﱾ�������|(zh��)��
����2������(�����l����׃��ֻ��׃һ���l��)
����������Ч��ײ��Փ
����1������ӡ���ܡ���Ч��ײ
����(1)�����
�����܉�l(f��)����Ч��ײ�ķ��ӡ�
����(2)���
��������ӱ���ͨ�������߳������������ԽС����ͨ���Ӿ�Խ����׃�ɻ���ӡ�����D��
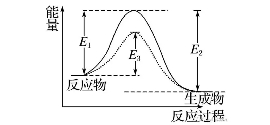
�����D�У�E1��������(y��ng)�Ļ�ܣ�ʹ�ô����r�Ļ�ܞ�E3������(y��ng)���E1��E2��(ע��E2���淴��(y��ng)�Ļ��)
����(3)��Ч��ײ
���������֮�g�܉����l(f��)���W(xu��)����(y��ng)����ײ��
����(4)����c���W(xu��)����(y��ng)���ʵ��P(gu��n)ϵ
������һ���l���£��������ռ�İٷ֔�(sh��)�ǹ̶���׃�ġ�����ӵİٷ֔�(sh��)Խ��λ�w�e��(n��i)����Ӕ�(sh��)Խ�࣬��λ�r�g��(n��i)��Ч��ײ�ĴΔ�(sh��)Խ�࣬���W(xu��)����(y��ng)����Խ�졣
����2������ӡ���Ч��ײ�c����(y��ng)���ʵ��P(gu��n)ϵ
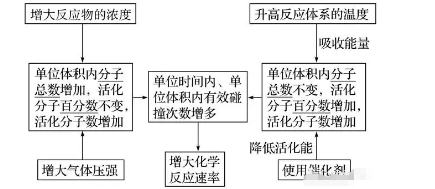
�������w����(y��ng)�wϵ�г�����Ԛ��w(�����c����(y��ng))�r������(y��ng)���ʵ�Ӱ�
����(1)����
��������“���Ԛ��w”�D→��������D→���|(zh��)��Ȳ�׃(����ӝ�Ȳ�׃)�D→����(y��ng)���ʲ�׃��
����(2)�㉺
��������“���Ԛ��w”�D→�w�e����D→���|(zh��)��ȜpС(����ӝ�ȜpС)�D→����(y��ng)���ʜpС��
�����������}�Nʿ
����1��Ӌ�����ʕr�����w�e�������|(zh��)����׃��ֵ���ԕr�g��
����2�����W(xu��)����(y��ng)���ʴ�С�ı��^����
��������ͬһ���W(xu��)����(y��ng)�ķ���(y��ng)�����ò�ͬ���|(zh��)��ʾ�r��(sh��)ֵ���ܲ�ͬ�����Ա��^����(y��ng)�Ŀ�������ֻ����(sh��)ֵ�Ĵ�С����Ҫ�M��һ�����D(zhu��n)����
����(1)����λ�Ƿ�y(t��ng)һ�������y(t��ng)һ���Q�����ͬ�Ć�λ��
����(2)�Q���ͬһ���|(zh��)��ʾ�����ʣ��ٱ��^��(sh��)ֵ�Ĵ�С��
����(3)���^���W(xu��)����(y��ng)�����c���W(xu��)Ӌ����(sh��)�ı�ֵ��
����3�������^���(f��)�s���P(gu��n)�ڷ���(y��ng)���ʵ��}Ŀ��“����ʽ”����
����(1)�������P(gu��n)����(y��ng)�Ļ��W(xu��)����ʽ��
����(2)�ҳ������|(zh��)����ʼ�����D(zhu��n)������ij�r������
����(3)����(j��)��֪�l���з���ʽӋ�㡣














